【小特集】
脳腸相関
現代では「心は脳に宿る」と考える人が多いですが,心は内臓とも関係しています。ここ数年,乳酸菌飲料が睡眠改善やストレス低減に効果があるという話を耳にされた方もいらっしゃるでしょう。今回は,脳と腸の不思議な関係について,4名の先生方に最新の知見をご紹介いただきます。(松田いづみ)
予測に基づき創発される脳と腸の機能

大平英樹(おおひら ひでき)
Profile─大平英樹
東京大学大学院社会学研究科博士課程満期退学。博士(医学)。2017年より現職。専門は生理心理学・認知神経科学。著書に『感情心理学・入門 改訂版』(編著,有斐閣)など。
脳と腸の歴史
ヒドラは,水に浮かぶ消化管ともいうべき動物です。筒状の体に網の目のような神経系を持ち,消化と代謝の能力を備えています。太古の昔,このような生物の神経が体の前部に集まり,環境の知覚と食餌運動を効率的に行うようになりました。脳は,こうした行動と栄養摂取を統合する制御装置として誕生したと考えられています[1]。
こうした進化的発想を背景に,19世紀初頭には脳と消化器官の関連が語られるようになりました。軍医ボーモントは怒りや不安が胃液分泌を変化させることを観察しました[2]。この発見は,ベルナールによる内部環境の恒常性という考えにつながりました[3]。19世紀後半に腸が独自の神経系を持つことが明らかになり,20世紀になるとベイリスらが,腸がホルモンを介して脳に情報を伝えることを見いだしました[4]。1970年代にはガーションが腸管神経系を第二の脳と呼び,脳と腸の相互作用を描きました[5]。ここにおいて,脳腸相関という概念が確立したのです。
脳と腸は予測に基づいて動く
脳と腸のコミュニケーションのうち神経経路では,腸の伸展や化学的変化が迷走神経と脊髄神経の求心線維により脳幹に伝えられ,脳からの出力は副交感(迷走)・交感(脊髄)神経を介して腸運動やホルモン分泌を調整します。液性経路では,グレリンやGLP-1などの消化に関するホルモンや,免疫細胞が分泌するサイトカインが血流を介して脳に到達し,摂食行動や気分に影響を与えます。一方,視床下部から分泌される副腎皮質刺激ホルモン放出ホルモン(CRH)をはじめとする脳由来の各種ホルモンが,腸の機能を多様に修飾します(図1)。本小特集で濱口豊太先生は,主にこの経路の機能とその異常を扱っています。
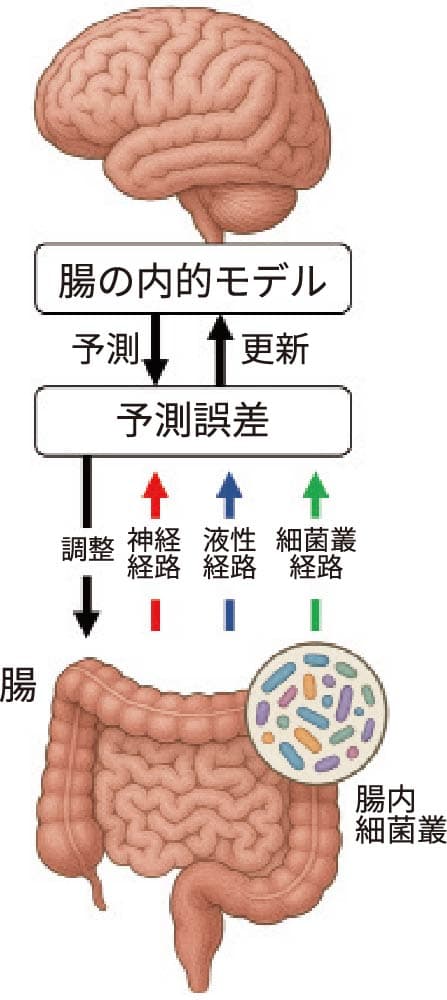
さらに2000年以降,腸内に存在する細菌などの多様な微生物(腸内細菌叢)が,短鎖脂肪酸やトリプトファン代謝物などを分泌し神経経路と液性経路を介して脳機能に影響すること,一方ストレスや情動による自律神経・ホルモン変化が腸運動や粘膜環境を変え,細菌叢の構成や機能を変容させることが明らかになりました[6]。本小特集で明和政子先生,高橋阿貴先生は,発達や情動行動における腸内細菌叢の意義についての先端的な知見を紹介しています。
こうした脳と腸の双方向的影響のメカニズムとして最近注目されているのが,フリストンにより提唱された予測的処理の理論です[7]。この理論では,脳は世界や自己を表現する生成モデルを構築し,到来する信号を予測していると考えます。予測と感覚信号の差異を予測誤差と呼び,これを最小化することで,内的モデルの更新と知覚の能動的な形成を行っていると考えられます。
この理論は視覚や聴覚などの知覚を対象としていますが,最近では腸を含む身体内部の過程,すなわち内受容感覚にも拡張されています[8]。例えば動物が,血糖値が低下してから空腹を感じて餌を探したとしても,餓死するリスクが高いでしょう。脳は生存や運動に伴うエネルギー需要に基づいて血糖低下を予測し,食餌行動を動機づけます。一方食後には,血糖値の上昇を予測し,消化関連ホルモンの分泌や腸の吸収速度を,自律神経を介して調整します。ここで,内的モデルが偏って非機能的であると,異常な摂食や不快感が知覚され,それが疾患にもつながります。
糖代謝の予測的処理
しかし,腸を含む内受容感覚が予測的処理の原理で制御されているということは,最近まで仮説に過ぎませんでした。そこで私たちは2021年から,JST-CRESTの研究費を得て『多様な迷走神経情報から創発する内受容感覚の脳統合』と題する,動物研究とヒト研究を並行して進めるプロジェクトを行っています。ここではその中から,糖代謝に関する最新の知見を紹介しましょう。
プロジェクトの代表である東北大学の佐々木拓哉教授は,内受容感覚の中枢であるラットの島皮質に,10分後の血糖値を予測するように活動するニューロン群を発見しました。これらのニューロンをムシモールで不活化すると,血糖値は,平均値は変わらないものの,分散が極端に大きくなり不安定化しました[9]。この知見は,ラットの島皮質が血糖値を予測に基づいてフィードフォワード的に制御していることを示唆します。
京都府立大学の岩崎有作教授は,アルロースという希少糖を用いて興味深い研究を行っています。アルロースは,カロリーはほぼ0ですが,腸から分泌され満腹感をもたらすGLP-1を誘導します[10]。これが腸の受容体と迷走神経により脳に伝達されると,セロトニンとバソプレッシン神経を介して,マウスの不安行動を低減し,他個体との社会的相互作用を促進しました。これらの結果は,腸からの信号が高次の内的モデルの機能に影響し,感情や行動を変容させることをうかがわせます。
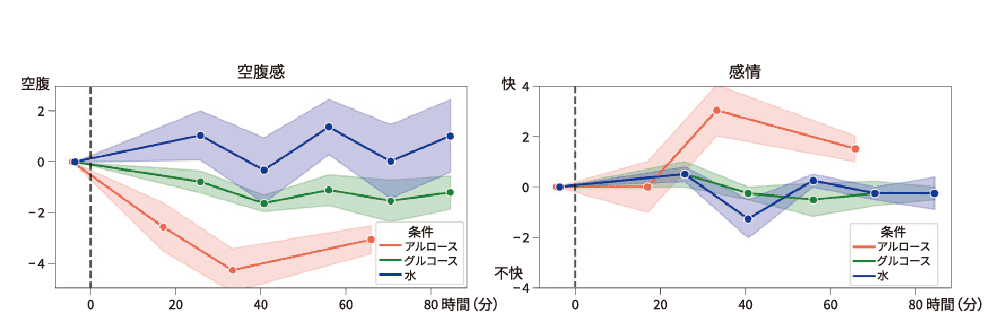
私たちは,ヒトにおいてこうした現象を検討するために,前夜から絶食し空腹状態の参加者に,60gのグルコース,アルロース,水(統制)を飲んでもらい,血糖値,主観評定,脳波,生理的反応を同時計測する実験系を構築しています。グルコースの投与は顕著な血糖値上昇を導きますが,空腹感や感情にはほとんど影響しません。これは,体内で生じる生理的変化が予測どおりであるので無視されるためと思われます。一方アルロース投与はGLP-1誘導により満腹信号を脳に伝え,大きな正の予測誤差を惹起すると考えられます。これが,劇的な空腹感の減退と快感情を誘発します(図2)。この知見は,ヒトにおいても糖代謝が予測的処理に従うことを示唆しています。ただし,この人工的な快感情が依存などの問題につながらないかは,慎重に検討する必要があります。
脳腸相関は,もはや頑健な科学的事実です。今後は本稿で述べたような,その背景にあるメカニズムやアルゴリズムに踏む込むことで,心理学においても重要なトピックとなっていくと考えられます。
文献
- 1.Furness, J. B., & Stebbing, M. J. (2018) Neurogastroenterol Motil, 30(2), e13234. ただしこの生物観には異論もある。
- 2.Beaumont, W. (1833) Experiments and observations on the gastric juice and the physiology of digestion. F. P. Allen.
- 3.Bernard, C. (1878) Leçons sur les phénomènes de la vie communs aux animaux et aux végétaux. J.-B. Baillière.(ベルナール/長野敬他訳 (1982) ベルナール:動植物に共通する生命現象.朝日出版社)
- 4.Bayliss, W. M., & Starling, E. H. (1902) J Physiol, 28, 325–353.
- 5.Gershon, M. D. (1998) The second brain. HarperCollins.(ガーション/古川奈々子訳 (2000) セカンドブレイン:腸にも脳がある! 小学館)
- 6.Sudo, N. et al. (2004) J Physiol, 558, 263–275.
- 7.Friston, K. (2010) Nat Rev Neurosci, 11, 127–138.
- 8.Barrett, L. F., & Simmons, W. K. (2015) Nat Rev Neurosci, 16, 419–429.
- 9.白鳥礼奈他(2025)後部島皮質による心拍と血糖値の調節[ポスター発表].第48回日本神経科学大会.
- 10.Iwasaki, Y. et al. (2018) Nat Commun, 9, 113.
- *COI:本記事に関連して開示すべき利益相反はありません。
PDFをダウンロード
1




